Les colonnes LC Raptor de Restek étaient les premières à associer la rapidité des analyses qu’autorisent les particules superficiellement poreuses ("SPP" ou "core-shell") avec le pouvoir de résolution lié à la grande sélectivité des colonnes USLC (Ultra Selective Liquid Chromatography). Elles permettent des séparations plus faciles avec des temps d’analyse plus courts sur des instruments HPLC standard. La gamme Raptor a ensuite évolué pour appliquer les mêmes caractéristiques de rapidité, d’efficacité et de sélectivité aux analyses UHPLC avec des colonnes contenant des particules de 1.8 μm. Plus d’informations sur les colonnes LC Raptor sur www.restek.com/raptor
En développant cette colonne, la priorité était de proposer une nouvelle version de notre phase Biphenyl, l’une des plus innovantes du marché, particulièrement appréciée pour son aptitude à séparer les composés difficiles à résoudre ou pour lesquels les phases C18 ou de type phényl ne sont pas assez résolutives ou rétentives. Les colonnes Raptor Biphenyl s’avèrent ainsi extrêmement utiles pour obtenir des séparations rapides pour des applications de bioanalyse ou des analyses de substances médicamenteuses et de leurs métabolites, en particulier si celles-ci nécessitent une détection par spectrométrie de masse. La rétention plus forte des composés habituellement peu retenus favorise l’ionisation ; la sélectivité plus élevée évite l’utilisation de phases mobiles complexes peu compatibles avec la détection par MS.
En 2005, Restek a découvert pour la première fois les avantages du ligand Biphenyl et, grâce à son expertise, a pu optimiser les propriétés des phases "SPP" associées à cette phase unique de type phényle afin de répondre aux exigences de rentabilité des laboratoires.
Caractéristiques :
|
 |
Type de phase stationnaire :
Phényle (L11)
Type de ligand :
Biphenyl
Particules :
Silice de 1.8 μm, 2.7 μm, ou 5 μm superficiellement poreuse ("SPP" ou "core-shell")
Porosité :
90 Å
Surface spécifique :
125 m2/g (1.8 μm),
130 m2/g (2.7 μm),
or 100 m2/g (5 μm)
|
Profil d'interactions :

Interactions principales :
- Polarisabilité
- Dispersion
Interaction secondaire :
|
Conditions d'utilisation :
Gamme de pH : 1.5–8.0
Température max. : 80 °C
Pression max. : 1 034 bar/15 000 psi* (1.8 μm),
600 bar/8 700 psi (2.7 μm); 400 bar/5 800 psi (5 μm)
* Pour une durée de vie maximale, la pression maximale recommandée pour les particules de
1.8 μm est 830 bar/12 000 psi.
Propriétés :
- Rétention plus forte des composés dipolaires, insaturés ou conjugués.
- Plus sélective en association à des phases mobiles à base de méthanol.
- Plus grande sensibilité en LC-MS.
La phase Biphenyl s’impose quand :
- Une colonne C18 n’est pas suffisamment sélective
- Une plus forte rétention des composés aromatiques hydrophiles
est recherchée.
Profil de rétention :

Analytes-cibles :
Fonctionnalités des analytes-cibles :
- Aromatiques hydrophiles
- Dipôles forts
- Acides de Lewis
- Dipolaires, insaturés ou conjugués
- Composés cycliques avec groupes électroattractifs
|
Sélectivité plus grande vis-à-vis des composés aromatiques par rapport aux colonnes de type phényl-hexyl conventionnelles
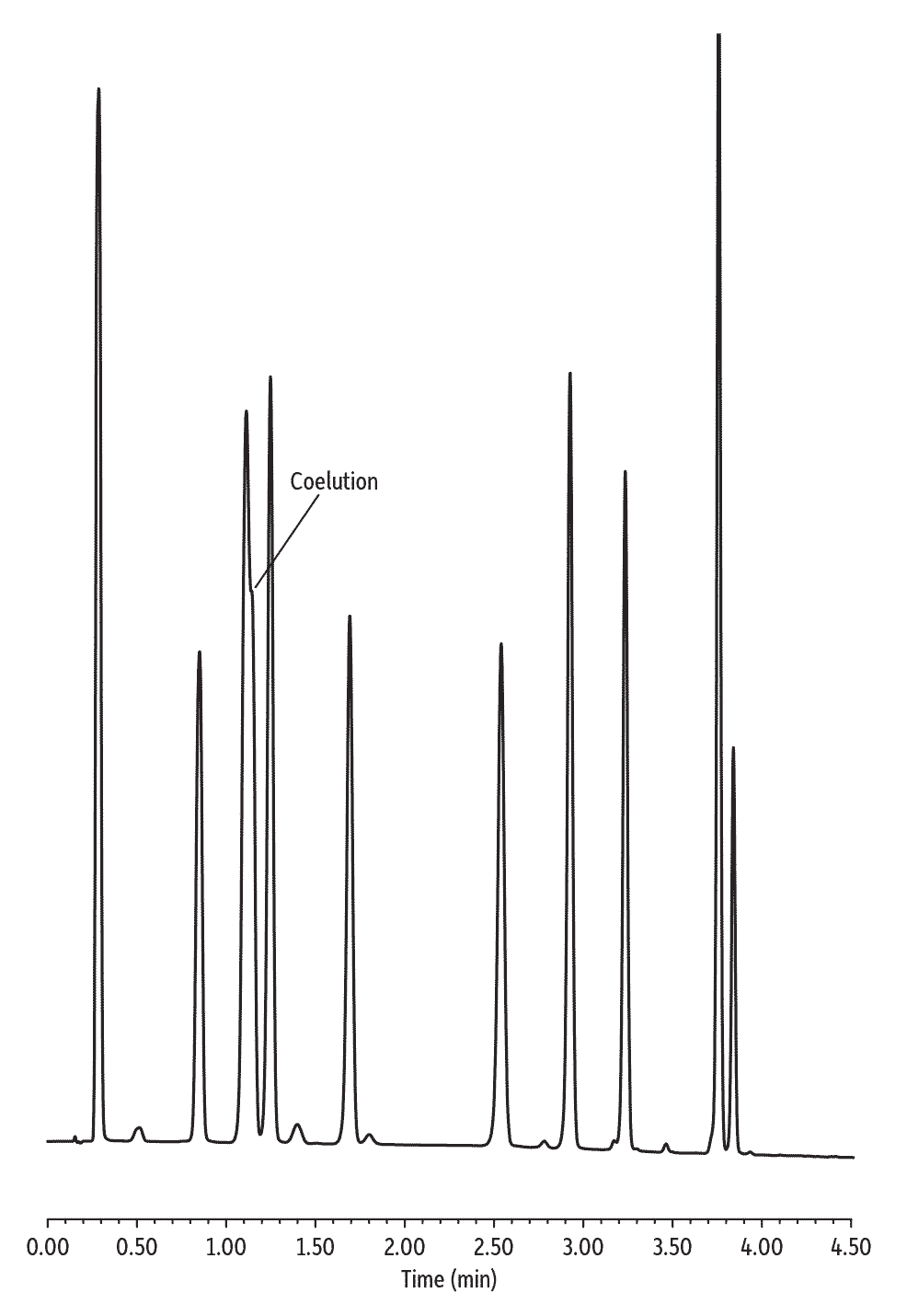
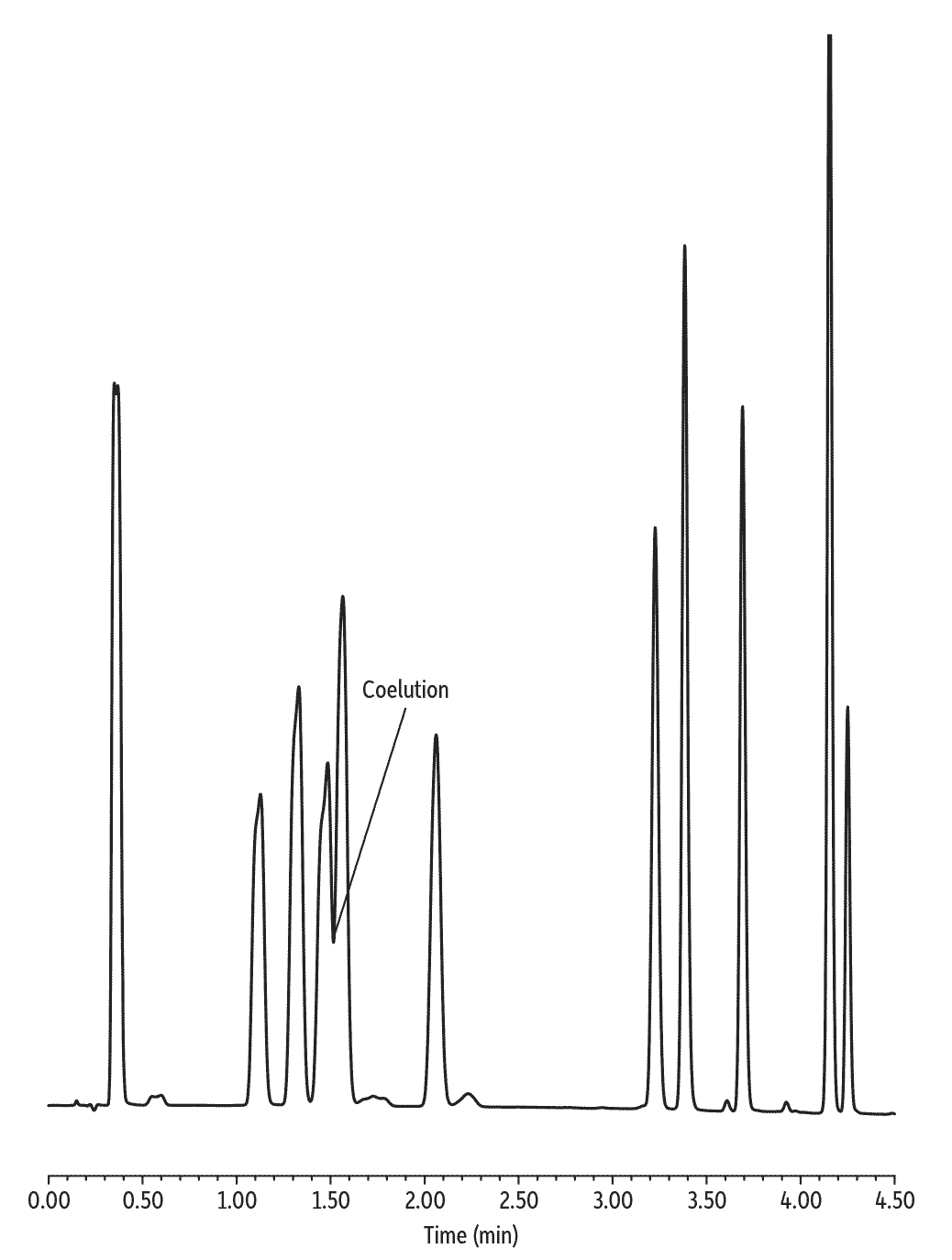
Les colonnes SPP "core-shell" contiennent souvent des phases stationnaires phényl-hexyl mais le ligand Biphenyl innovant mis au point par Restek représente la dernière génération des phases à base de groupements phényl. Il offre une meilleure sélectivité que les phases de type phényl-hexyl du marché vis-à-vis des composés aromatiques [1] et un plus grand degré de dispersion que les phases de type phényle. Les colonnes Raptor Biphenyl permettent ainsi de séparer plus facilement les composés aromatiques (Figures 1 et 2) trop rapidement élués ou difficilement séparables avec des phases de type C18 ou phényle.
1. In-house testing based on: M.R. Euerby, P. Petersson, W. Campbell, W. Roe, Chromatographic classification and comparison of commercially available reversed-phase liquid chromatographic columns containing phenyl moieties using principal component analysis, J. Chromatogr. A 1154 (2007) 138–151.
Figure 1 : Les colonnes Raptor Biphenyl offrent une meilleure sélectivité que les colonnes SPP de type phényle vis-à-vis des composés aromatiques.

Une référence en matière de qualité et de longévité
Pression stable :
L’un des principaux avantages des colonnes "SPP" par rapport aux colonnes conventionnelles à particules complètement poreuses est leur aptitude à réaliser de bonnes séparations rapidement à des vitesses linéaires plus élevées. Des vitesses linéaires importantes peuvent toutefois générer des contrepressions plus fortes. Les colonnes Raptor ont été conçues pour supporter plus durablement que les autres colonnes "SPP" du marché les pressions nécessaires aux analyses rapides (Figure 3).
Figure 3 : Soumises à de fortes pressions, les colonnes de type phényl-hexyl du marché voient rapidement leur efficacité s’effondrer, alors que l’efficacité des colonnes Raptor Biphenyl demeure inchangée après 3 000 injections.

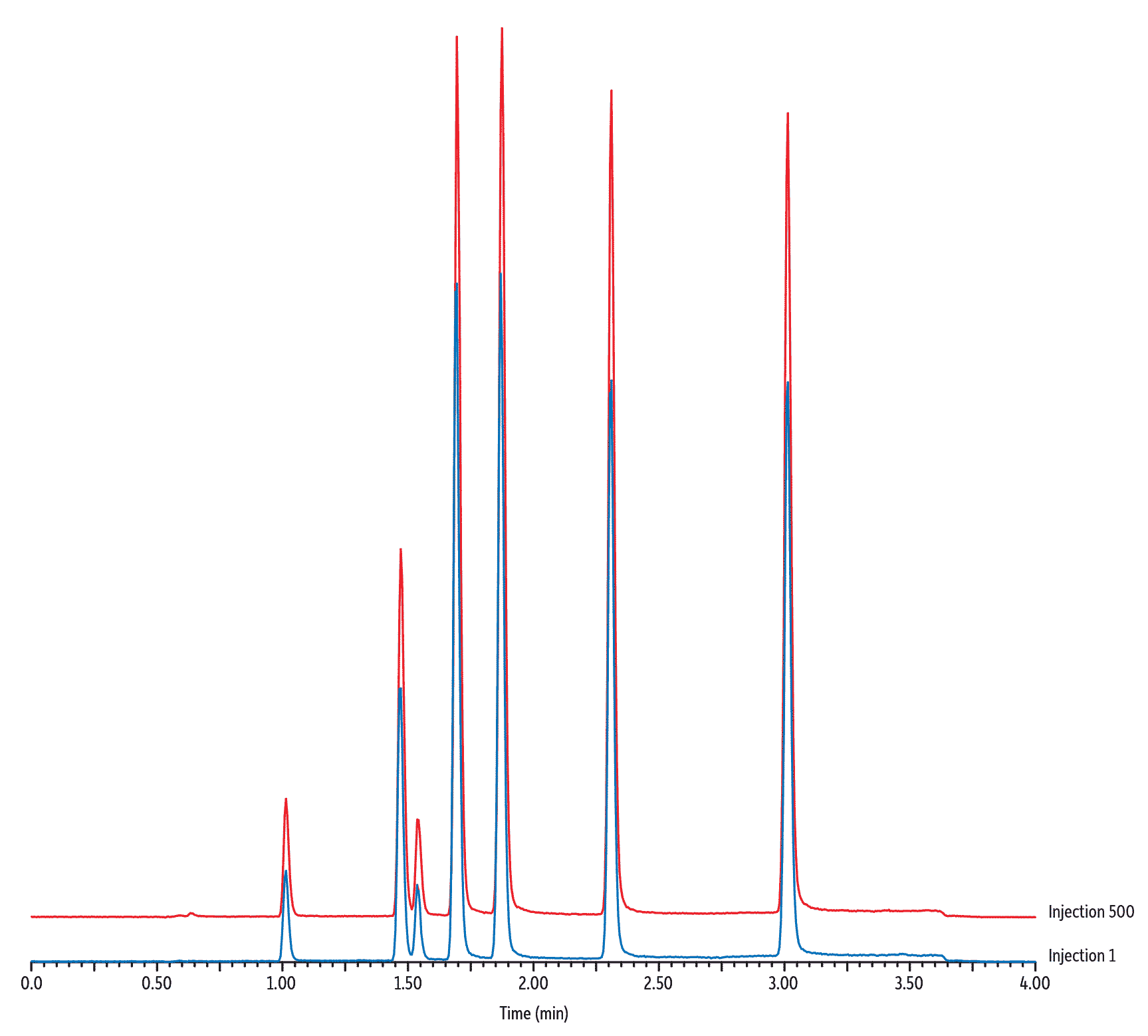
Reproductibilité :
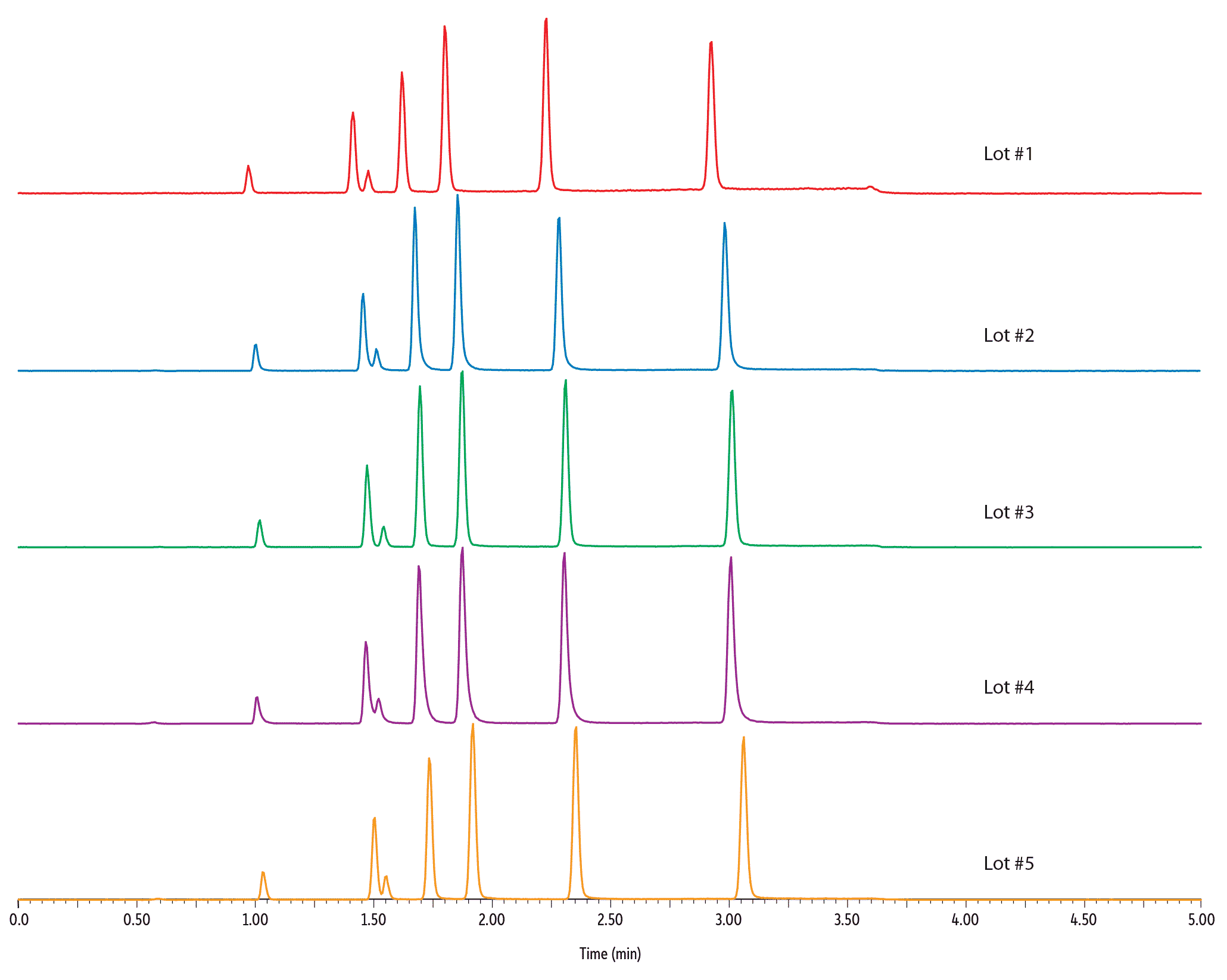
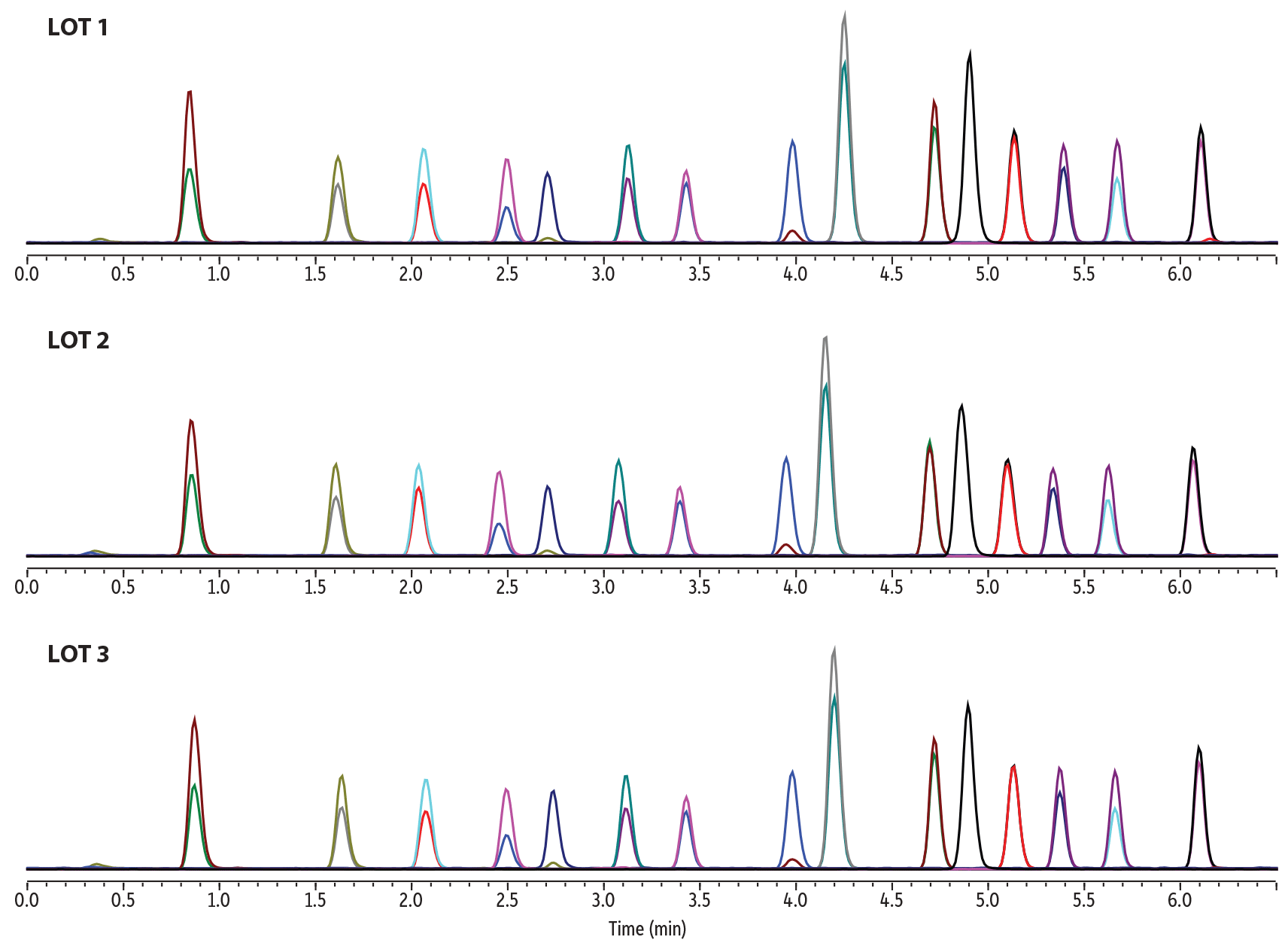
Les colonnes Raptor Biphenyl offrent une sélectivité exceptionnelle et permettent des analyses rapides de façon reproductible. Leur robustesse et leur répétabilité sont des paramètres essentiels. La silice, le procédé de greffage, le remplissage, la conception des raccords et des frittés, tout a été étudié pour garantir une extraordinaire reproductibilité d’une injection à l’autre (Figure 4) et d’un lot à l’autre (Figure 5), quelles que soient les dimensions de la colonne (Figure 6). Des spécifications de contrôle qualité (CQ) encore plus strictes ont également été adoptées pour assurer la stabilité des temps de rétention, indispensable aux analyses MRM.
Figure 6 : Quelles que soient les dimensions, les colonnes Raptor sont suffisamment robustes pour dépasser largement les 1 000 injections, même soumises aux fortes pressions propres à l’UHPLC.

Conçues pour répondre aux exigences de rentabilité des laboratoires d’analyses
Depuis plus de dix ans, la phase Biphenyl Restek est la phase de choix pour les analyses LC, de par sa forte rétentivité, sa grande sélectivité et sa robustesse, très appréciées pour par exemple la séparation en phase inverse de substances médicamenteuses et de leurs métabolites. Combinant ces qualités aux avantages des particules "SPP", les colonnes Raptor Biphenyl permettent aux laboratoires des analyses encore plus rapides pour une large gamme de molécules.
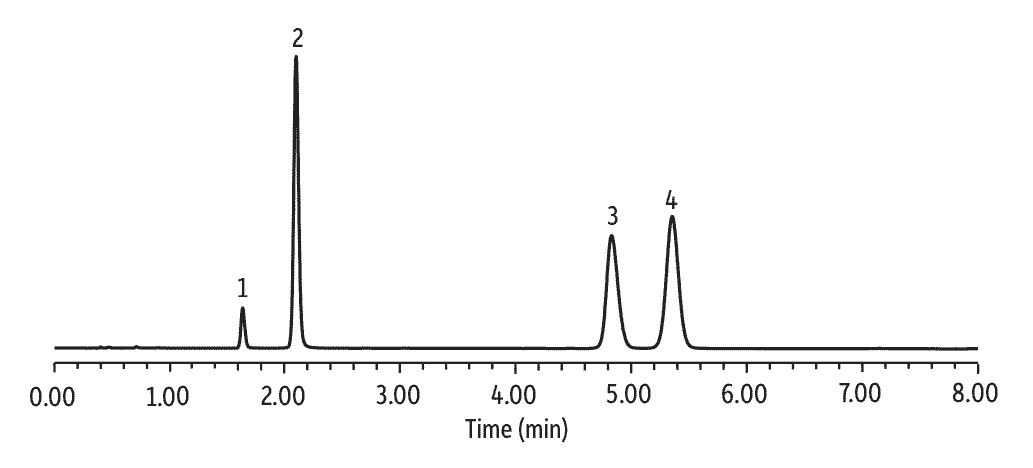
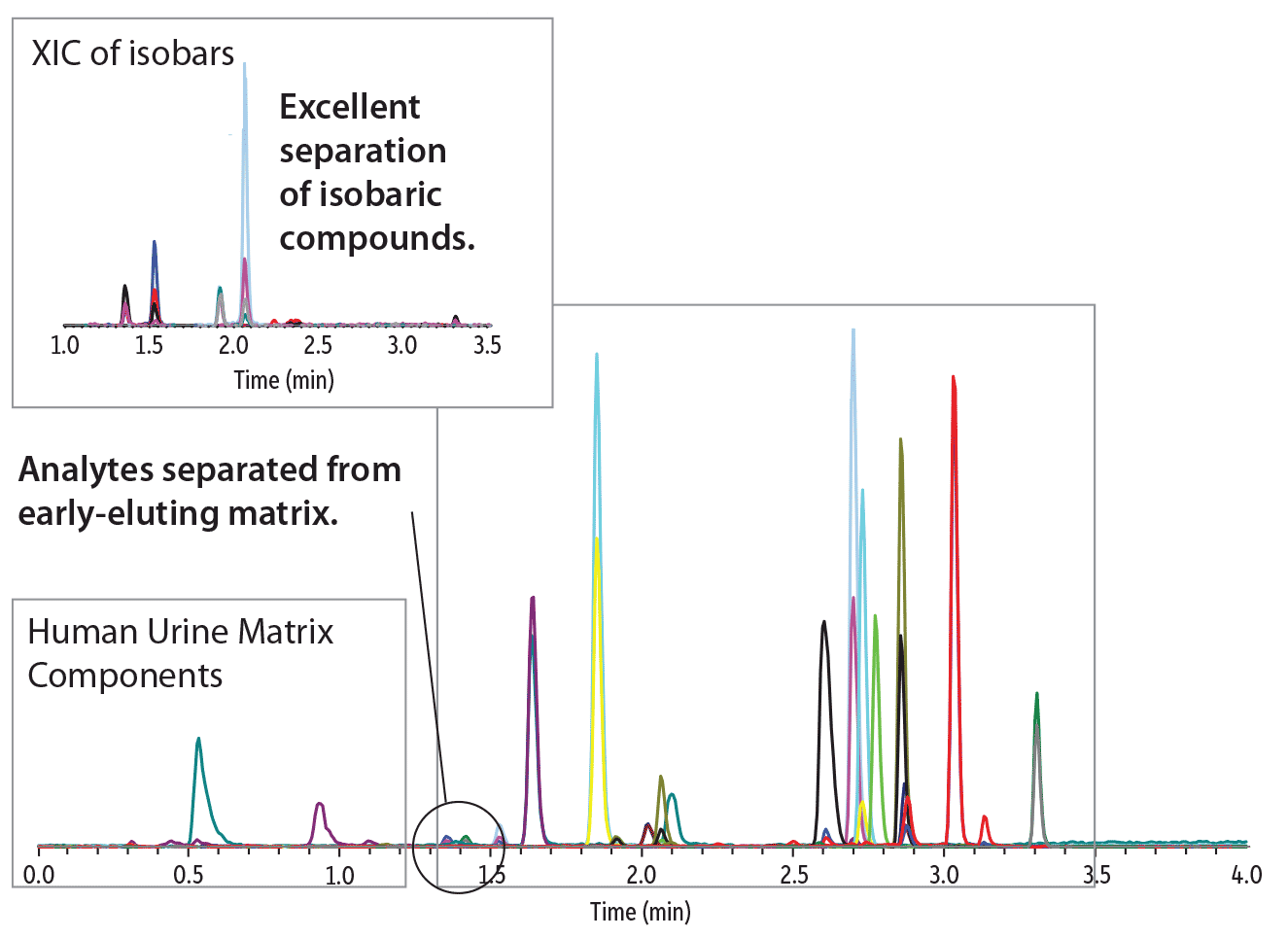
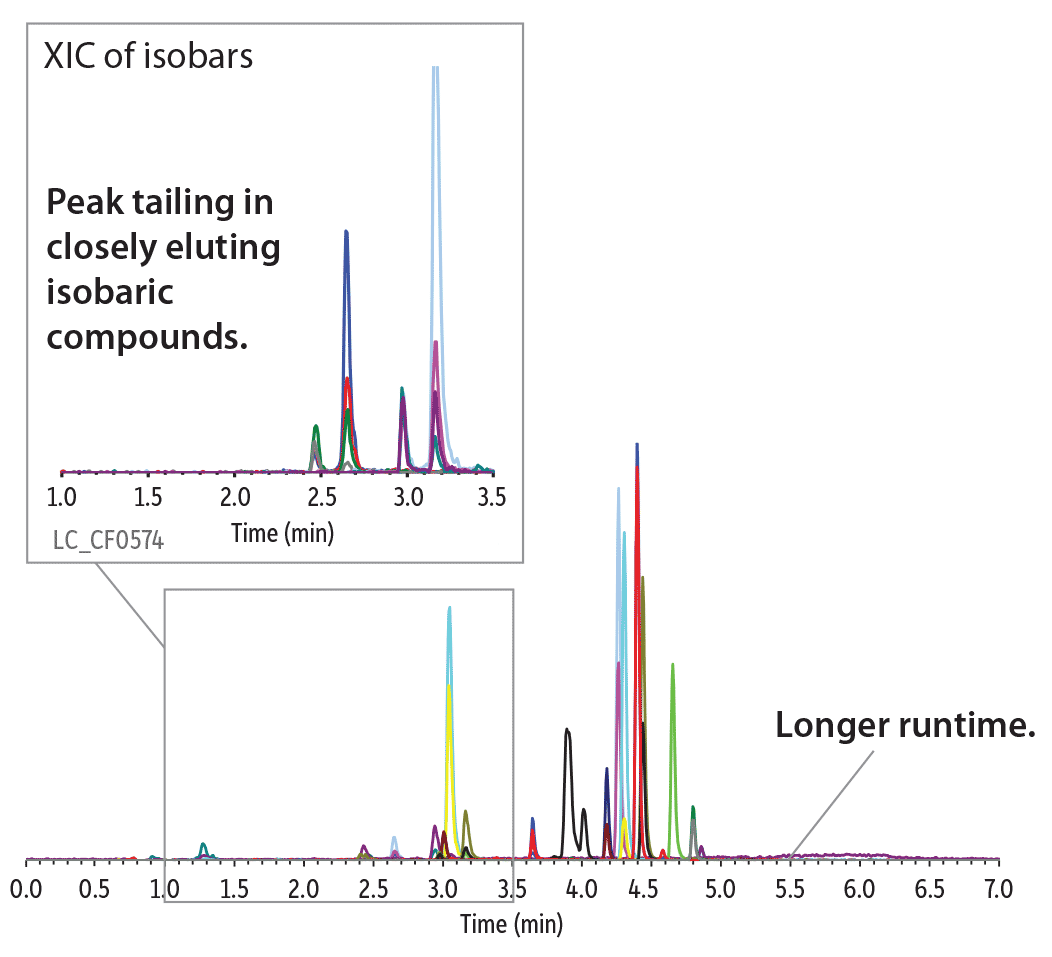
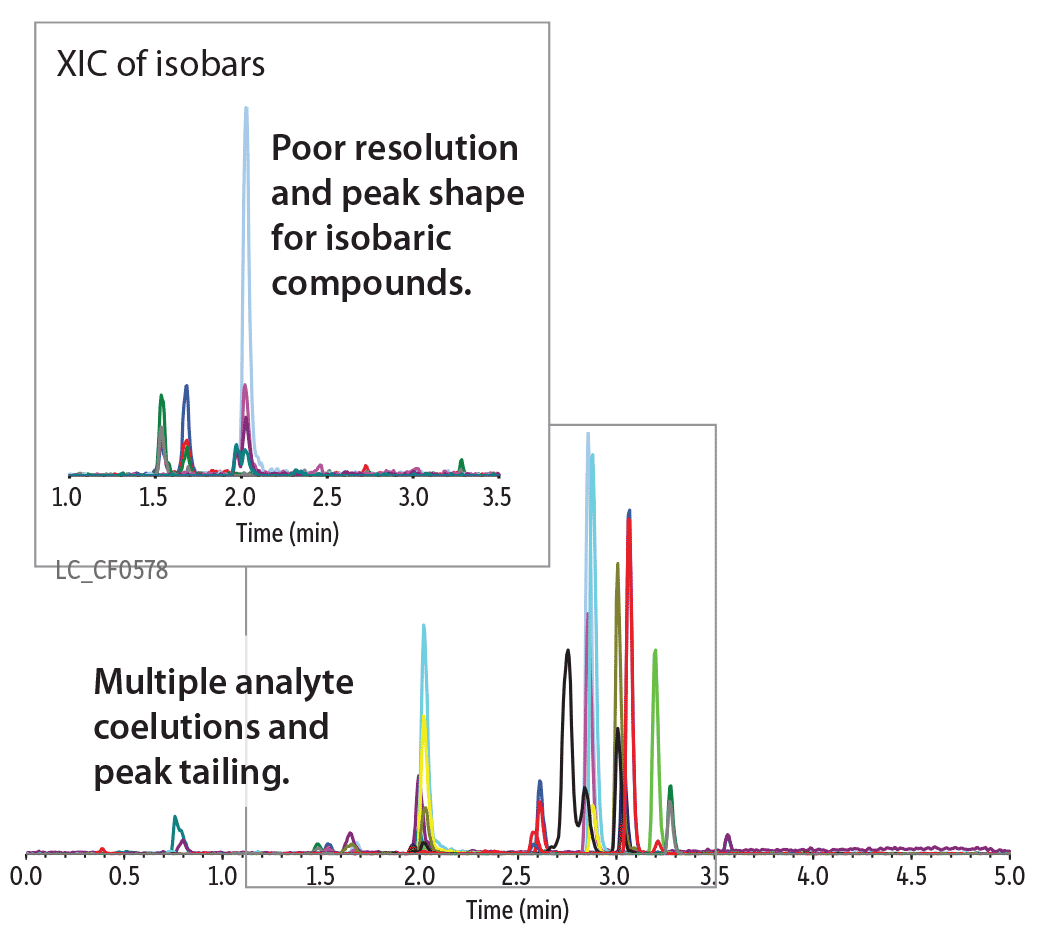
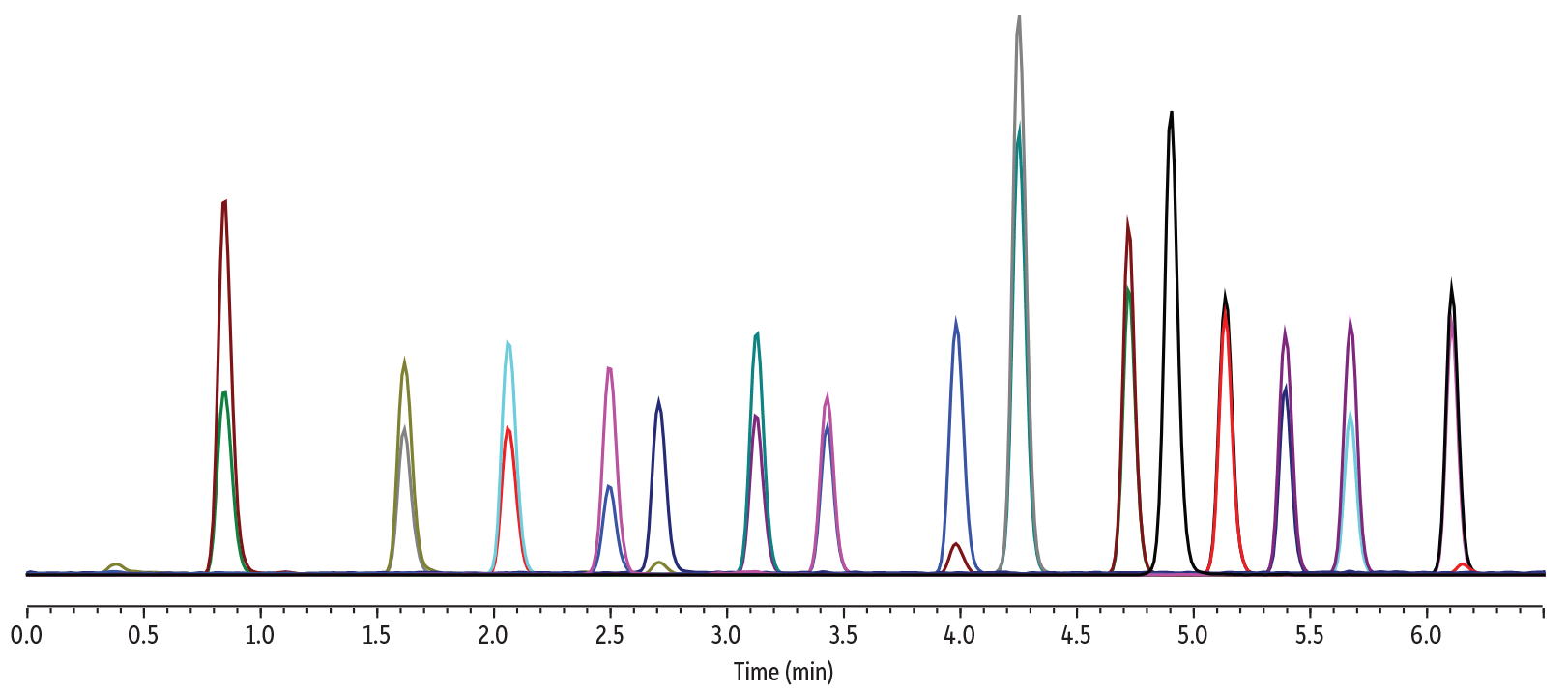
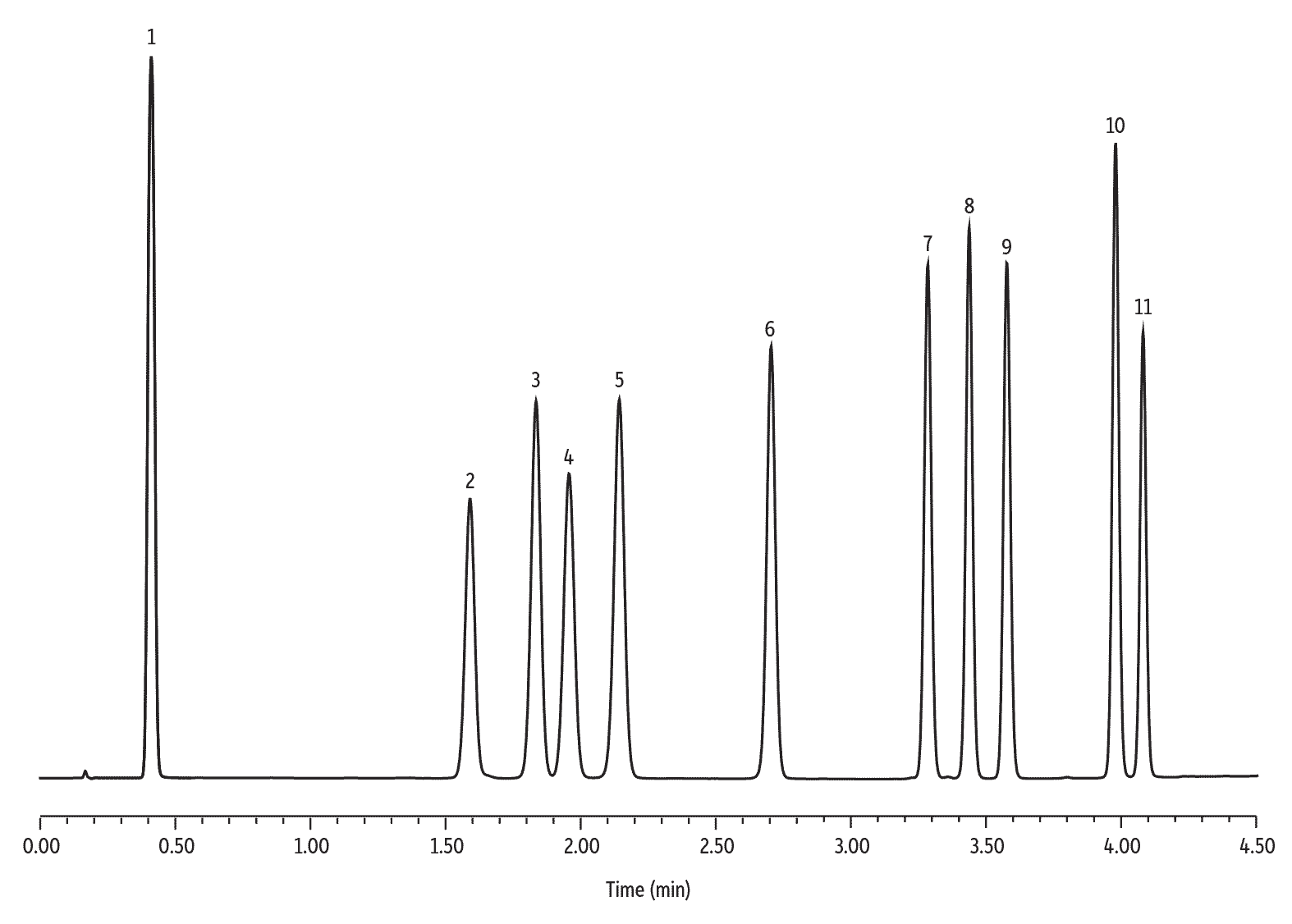
Screening d’analgésiques dans l’urine en moins de 3.5 minutes
Un screening d’analgésiques peut se révéler difficile à optimiser et à reproduire du fait de la sélectivité insuffisante des phases de type C18 ou phényl-hexyl. La colonne Raptor Biphenyl permet quant à elle un screening en moins de 5 minutes avec une résolution totale des isobares (Figure 7). Avec la plupart des colonnes du marché, les pics traînent, les temps d’analyse sont longs et les coélutions nombreuses. Seule la colonne Raptor Biphenyl offre la sélectivité et les propriétés indispensables à cette analyse difficile.
Résolution complète des bisphénols grâce à la sélectivité du ligand Biphenyl, sans ajustement de la phase mobile
Pour les analyses de santé et de sécurité alimentaire comme l'évaluation des bisphénols dans les produits de consommation, la rapidité, la fiabilité et la simplicité sont essentielles. La colonne Raptor Biphenyl est capable de séparer un grand nombre de composés rapidement (par exemple, 15 bisphénols en 8 minutes, voir ci-dessous [Figures 8 et 9]) avec un simple gradient de phases mobiles ne nécessitant AUCUN additif. Lorsqu’un retour à la ligne de base est nécessaire pour la détection en UV ou pour une productivité maximale des analyses en spectrométrie de masse, en particulier si la rapidité, la confiance et la simplicité sont essentielles, la colonne Raptor Biphenyl est le choix idéal.
Analyse rapide des antibiotiques contenant du soufre
Même avec les particules ultra efficaces utilisées en UHPLC, les colonnes ordinaires de type C18 ou phényle ne permettent pas de séparer les sulfonamides avec retour à la ligne de base. La colonne Raptor Biphenyl offre une meilleure sélectivité qui permet de séparer facilement ces composés difficiles (Figure 10) en moins de 5 minutes.
Expérimentez la Selectivity Accelerated. Demandez un devis pour une colonne Raptor Biphenyl.